コントロールされた増殖可能なのだろうか?
Self-amplifying RNA vaccines for infectious diseases
Kristie Bloom, Fiona van den Berg & Patrick Arbuthnot
Gene Therapy volume 28, pages 117–129 (2021)
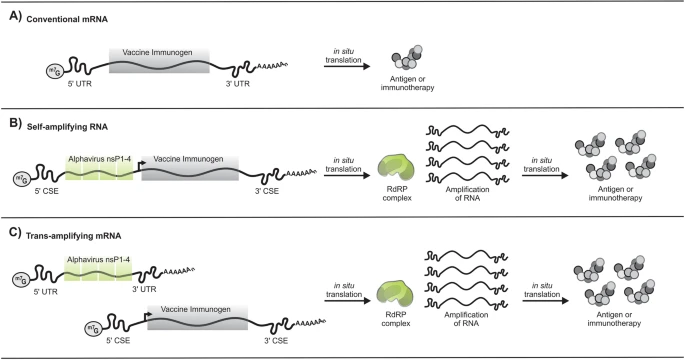
A 5′ cap (m7G) と poly A tail はすべてのRNA転写産物に共通である。A 従来のmRNAは、ワクチンの免疫原とそれに付随する5′および3′UTRをコードしている。抗原や免疫療法は、非複製の転写物から翻訳される。
B 自己複製RNAは、5′および3′のCSE配列、nsP1-4遺伝子、サブゲノムプロモーター、およびワクチン免疫原をコードする。in situ翻訳後、nsP1-4タンパク質はRdRP複合体を形成し、CSE配列を認識してワクチンをコードする転写産物を増幅する。その結果、細胞内に抗原や免疫療法が蓄積されることになる。
C トランス増幅型mRNAは、自己増幅型RNAと同様の効果を得るために、2つの異なる転写産物を用いる。5′および3′UTRに挟まれたnsP1-4遺伝子をコードする従来のmRNAは、ウイルスのCSE配列、サブゲノムプロモーター、およびワクチン免疫原をコードする別の転写産物と一緒に送出される。従来のmRNAをin situで翻訳するとRdRP複合体が形成され、続いてワクチンをコードする転写産物が増幅され、抗原の蓄積や免疫療法が行われることになる。
UTR untranslated region, CSE conserved sequence elements, nsP1–4 nonstructural proteins 1–4, RdRP RNA-dependent RNA polymerase.
| Property | Advantage | Disadvantage |
| 効能・効果 | 従来のタンパク質ベースのワクチンに匹敵する有効性を持つ | プライム/ブースト投与が必要な場合もある |
| その場で高いレベルのRNA増幅が行われる | ||
| saRNAを持続的に高レベルで増幅・発現させた場合の影響についてはほとんど情報がない | ||
| saRNAの活性は細胞質内で起こるため、DNAワクチンのような核移植は必要ない | ||
| 発現した抗原に対して、体液性および細胞性の反応が誘発される | ||
| 前臨床試験では、感染症に対する防御効果が確認されている | ||
| 安全性 | 構造タンパク質のウイルス遺伝子がsaRNAレプリコンから取り除かれており、ウイルスのアセンブリーを防ぐことができる | RdRP複合体の免疫原性に関する情報はほとんどない。 |
| 細胞質内で作用するため、統合の危険性がない | これまでの臨床データが少ない | |
| 合成 | GMP in vitro transcriptionを用いた大規模な合成に適している | |
| 異なる抗原に対する新しい配列を容易に合成することができる | ||
| 多価性または多病原性の配列を柔軟に組み込むことができる | ||
| NVVによるデリバリー | 非ウイルス性ベクターを用いた送達が可能 | 通常、組織特異的な投与は行われない |
| 大規模な合成が可能な製剤 | NVVsとsaRNAの免疫原性のバランス | |
| 筋肉内、皮内、または皮下注射後の送達部位での発現 |
www.DeepL.com/Translator(無料版)で翻訳しました。