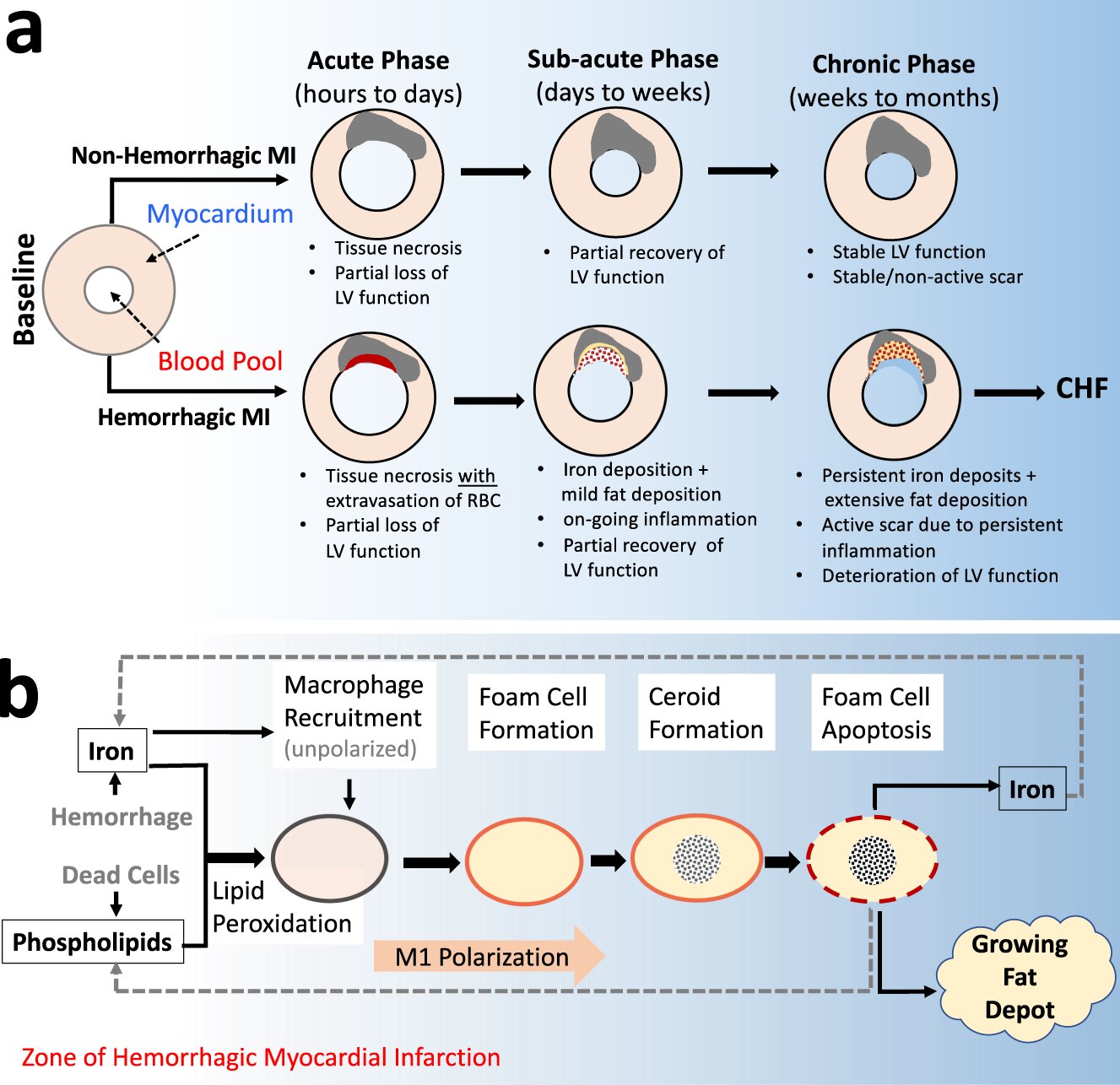
Intramyocardial hemorrhage drives fatty degeneration of infarcted myocardium
nature communications Published: 27 October 2022
心筋に栄養を送る動脈の突然の閉塞は、世界中で数百万人の心臓発作(心筋梗塞、MI)の原因となっている。再灌流により心筋梗塞患者は即死を免れるが、その約50%は慢性心不全を発症し、5年以内に死亡する。しかし、なぜ心不全に移行する患者と移行しない患者がいるのかは、いまだ不明である。再灌流心筋梗塞の大動物モデルを用いて、再灌流障害の最も有害な形態である心筋内出血(再灌流ST上昇型心筋梗塞患者の約40%に認められる)が梗塞治癒を遅らせ、心筋梗塞の持続的脂肪変性に中心的に関与し、心臓の悪いリモデリングを引き起こすことを明らかにする。特に、出血性心筋梗塞部位の脂肪変性は、鉄によるマクロファージの活性化、過酸化脂質、泡沫細胞形成、セロイド生成、泡沫細胞のアポトーシス、鉄の再利用に起因することを明らかにした。また、出血性心筋梗塞領域内の鉄を適時に減少させることで、脂肪浸潤を減らし、心臓を好ましいリモデリングへと導くことも明らかにした。これらの知見は、なぜすべての心筋梗塞ではなく一部の心筋梗塞が心不全になるのかを明らかにし、心筋梗塞の大きさに関係なく心筋梗塞後の心不全を緩和する治療戦略の可能性を示すものである。
www.DeepL.com/Translator(無料版)で翻訳しました。