Role of unfolded proteins in lung disease
https://thorax.bmj.com/content/early/2020/10/18/thoraxjnl-2019-213738
肺は様々な環境毒素(タバコの煙、大気汚染、アスベストを含む)や病原体(細菌、ウイルス、真菌)にさらされており、ほとんどの呼吸器疾患は局所的または全身的な低酸素に関連しています。これらの有害因子はすべて、小胞体(ER)ストレスの引き金となります。
小胞体は、分泌および膜タンパク質の合成のための細胞内の重要な部位であり、それらの折り畳み、複合体への組み立て、輸送、および分解を制御しています。
unfolded protein response
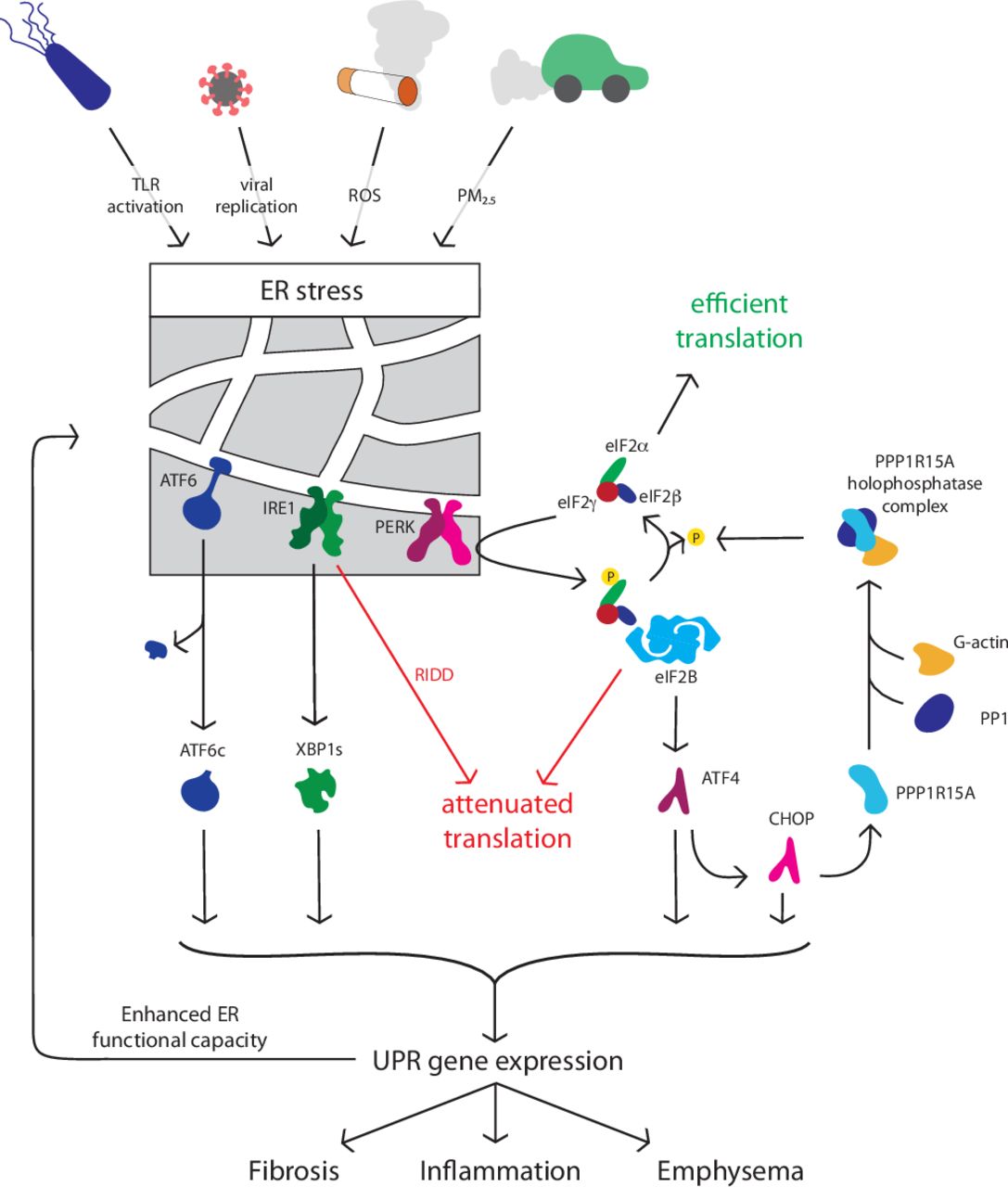
小胞体内にmisfolded proteinが蓄積されると、小胞体ストレスが生じ、unfolded protein response (UPR)が活性化されます。UPRのエフェクターは一時的にタンパク質合成を低下させ、一方で、 misfolded proteinの分解を促進し、ERの折り畳み能力を増加させる。成功すれば、恒常性が回復し、タンパク質合成が再開するが、ERストレスが持続すると、細胞死経路が活性化する。
ERストレスとその結果生じるUPRは、様々な肺障害で発生し、その結果は多くの呼吸器疾患において重要な役割を果たしています。UPRは、いくつかの呼吸器疾患を持つ患者の気道とそれに対応する実験モデルでトリガーされます。ERストレスは、肺線維化の開始および進行に関与しており、閉塞性肺疾患(特に喘息)、肺感染症(一部のウイルス感染症および嚢胞性線維化気道の設定)、および肺癌においてERストレスが起こることを示唆する証拠が蓄積されている。疾患モデルにおける UPR の役割を調べるために多くの低分子阻害剤が使用されてきたが、これらのツールの多くは複雑で標的外の効果を持つため、そのような薬理学的薬剤の影響に基づく結論を支持するためには、追加の証拠(例えば、遺伝子操作によるもの)が必要とされるかもしれない。UPRの異常な活性化は、疾患の発症や進行に関連している可能性があるが、これらのプロセスに関連する context-specific なメカニズムや疾患特異的なメカニズムについての理解は、現時点では不完全である。しかし、UPRがERストレスから身を守り、様々な呼吸器疾患に影響を与えることが明らかになってきており、治療介入戦略のターゲットとして注目されています。
<hr>
UPRと特発性肺線維症
肺線維性肺疾患におけるERストレスとunfolded protein応答。肺線維症では、タバコの煙、アスベスト、粒子状物質またはウイルスなどの引き金は、遺伝的に素因を持つ宿主(例えば、サーファクタントタンパク質変異、MUC5B多型)においてERストレスを誘発する可能性がある。これは、アポトーシスおよびepithelial mesenchymal transition (EMT)と関連している。組織低酸素は、患部のERストレスをさらに促進する可能性がある。
ER、小胞体;MUC5B、ムチン5B;UPR、unfolded protein response。
www.DeepL.com/Translator(無料版)で翻訳しました。
<hr>
UPRと喘息
 |
| 説明を追加 |
喘息におけるERストレスとunfolded protein response応答。喘息では、ハウスダストマイト、ウイルス性または真菌性病原体、およびタバコの煙などの誘因は、遺伝的に素因を持つ(例えば、ORMDL3多型)宿主においてERストレスを引き起こす可能性があります。これは、炎症、アポトーシス、粘液の過分泌に関連しており、気道反応性およびリモデリングにつながる。
ER、小胞体;UPR、unfolded protein response。
<hr>
UPRとCOPD
COPDを対象とした大規模なGWASやシークエンス研究にもかかわらず、ERストレスやUPRとの明確な遺伝的関連性は明らかにされていない。CSは気道上皮細胞においてERストレスを誘導することができるが、これは機序的な関連性とは言えず、複数の細胞ストレス経路がCSによって開始される。Minらは、UPRのIRE1とATF6については調査していないが、COPD患者の肺では免疫ブロッティングによりリン酸化されたeIF2αとCHOPの発現が増加していることを報告している。Hassanらは、COPD患者の単球においてmiR199a-5pの発現低下がBiP、ATF6、XBP1sの発現増加の裏付けとなっていることを報告しているが、これは興味深い知見であるが、肺の病理学的意義は不明である。マウスモデルもまた、肺気腫におけるERストレスの役割の可能性を示唆しているが、そのようなモデルがヒトの疾患をどのように再現するかは議論の余地がある。4-PBAは、CS誘発性肺気腫のマウスモデルにおいて部分的に保護され、ヘム消去タンパク質であるヘモペキシンで処理されたマウスは、臭素吸入に対するERストレス、気道線維化、および肺気腫の発症がコントロールマウスよりも少なかった15。
このように、全体的に見ると、UPR は COPD の文脈で活性化されている可能性があるが、COPD 病因に対する UPR の寄与は現在のところ不明である。
<hr>
COPDのところがオチ

0 件のコメント:
コメントを投稿